Часть I
1. Коррозия – это самопроизвольное разрушение металлов и сплавов под действием окружающей среды.
2.
Типы коррозии

3.Условия протекания электрохимической коррозии:
1) Влага
2) Кислород атмосферный
4. Вред, который наносит коррозия:
а) страдает экология;
б) теряется 25% всего произведенного железа;
в) портятся металлические изделия;
г) страдает здоровье людей.
5. Заполните таблицу «Защита металлов от коррозии».

Часть II
1. Запишите уравнение реакций, протекающих на воздухе с литием, лишённым вазелиновой защиты.

2. «По крыше выложили жесть» (В. В. Маяковский). Опишите процессы, происходящие с белой жестью при нарушении оловянной защиты.

Железо ржавеет.
3. Заполните таблицу «Свойства некоторых легированных сталей и их примесей».

4. Опишите, какие способы защиты металлов от коррозии используются у вас в ванной комнате и на кухне.
Эмаль, лаки, краски.
5. Напишите синквейн о коррозии металлов.
а) Коррозия
б) Вредный, портящий
в) Разрушает, мешает, портит
г) Вредный процесс, разлагает
д) Металлы
6. Перечислите наиболее часто используемые способы защиты от коррозии изделий, изображенных на рисунках.
а) Покрытие сплавом мельхиора.
б) Эмаль
в) Легирование стали ванадием.
г) Легирование хромом
д) Лужение оловом
е) Легирование титаном
7. Приведите примеры электрохимических процессов (электрохимической коррозии), приносящих людям пользу.
1) Гальванотехника – нанесение покрытия в виде металлов и сплавов.
2) Электрофорез, электродиализ, электроосмос.
Электрохимическая коррозия — самый распространенный вид коррозии. Электрохимическая коррозия возникает при контакте металла с окружающей электролитически проводящей средой. При этом восстановление окислительного компонента коррозионной среды протекает не одновременно с ионизацией атомов металла и от электродного потенциала металла зависят их скорости. Первопричиной электрохимической коррозии является термодинамическая неустойчивость металлов в окружающих их средах. Ржавление трубопровода, обивки днища морского суда, различных металлоконструкций в атмосфере — это, и многое другое, примеры электрохимической коррозии.
К электрохимической коррозии относятся такие виды местных разрушений, как питтинги, межкристаллитная коррозия, щелевая. Кроме того процессы электрохимической коррозии происходят в грунте, атмосфере, море.
Механизм электрохимической коррозии может протекать по двум вариантам:
1) Гомогенный механизм электрохимической коррозии:
— поверхностный слой мет. рассматривается как гомогенный и однородный;
— причиной растворения металла является термодинамическая возможность протекания катодного или же анодного актов;
— К и А участки мигрируют по поверхности во времени;
— скорость протекания электрохимической коррозии зависит от кинетического фактора (времени);
— однородную поверхность можно рассматривать как предельный случай, который может быть реализован и в жидких металлах.
2) Гетерогенный механизм электрохимической коррозии:
— у твердых металлов поверхность негомогенная, т.к. разные атомы занимают в сплаве различные положения в кристаллической решетке;
— гетерогенность наблюдается при наличии в сплаве инородных включений.
Электрохимическая коррозия имеет некоторые особенности: делится на два одновременно протекающих процесса (катодный и анодный), которые кинетически зависимы друг от друга; на некоторых участках поверхности электрохимическая коррозия может принять локальный характер; растворение основного мет. происходит именно на анодах.
Поверхность любого металла состоит из множества короткозамкнутых через сам металл микроэлектродов. Контактируя с коррозионной средой образующиеся гальванические элементы способствуют электрохимическому его разрушению.
Причины возникновения местных гальванических элементов могут быть самые разные:
1) неоднородность сплава
— неоднородность мет. фазы, обусловленная неоднородностью сплава и наличием микро- и макровключений;
— неравномерность окисных пленок на поверхности за счет наличия макро- и микропор, а также неравномерного образования вторичных продуктов коррозии;
— наличие на поверхности границ зерен кристаллов, выхода дислокации на поверхность, анизотропность кристаллов.
2) неоднородность среды
— область с ограниченным доступом окислителя будет анодом по отношению к области со свободным доступом, что ускоряет электрохимическую коррозию.
3) неоднородность физических условий
— облучение (облученный участок — анод);
— воздействие внешних токов (место входа блуждающего тока — катод, место выхода — анод);
— температура (по отношению к холодным участкам, нагретые являются анодами) и т. д.
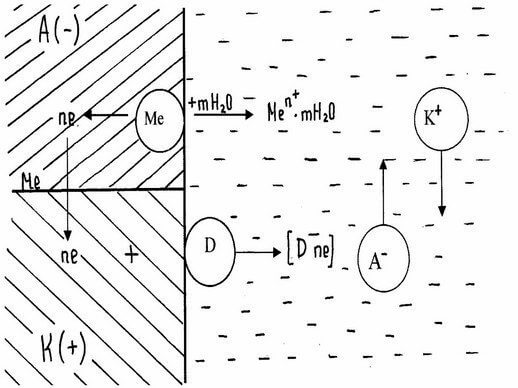
При работе гальванического элемента одновременно протекает два электродных процесса:
Анодный — ионы металла переходят в раствор
Происходит реакция окисления.
Катодный — избыточные электроны ассимилируются молекулами или атомами электролита, которые при этом восстанавливаются. На катоде проходит реакция восстановления.
O2 + 2H2O + 4e → 4OH — (кислородная деполяризация в нейтральных, щелочных средах)
O2 + 4H + + 4e → 2H2O (кислородная деполяризация в кислых средах)
2 H + + 2e → H2 (при водородной деполяризации).
Торможение анодного процесса приводит к торможению и катодного.
При соприкосновении двух электропроводящих фаз (например, мет. — среда), когда одна из них заряжена положительно, а другая отрицательно, между ними возникает разность потенциала. Это явление связано с возникновением двойного электрического слоя (ДЭС). Заряженные частицы располагаются несимметрично на границе раздела фаз.
Скачек потенциалов в процессе электрохимической коррозии может происходить из-за двух причин:
При достаточно большой энергии гидратации ионы металла могут отрываться и переходить в раствор, оставляя на поверхности эквивалентное число электронов, которые определяют ее отрицательный заряд. Отрицательно заряженная поверхность притягивает к себе катионы мет. из раствора. Так на границе раздела фаз возникает двойной электрический слой.
На поверхности металла разряжаются катионы электролита. Это приводит к тому, что поверхность мет. приобретает положительный заряд, который с анионами раствора образует двойной электрический слой.
Иногда возникает ситуация, когда поверхность не заряжена и, соответственно, отсутствует ДЭС. Потенциал, при котором это явление наблюдается называется потенциалом нулевого заряда (φN). У каждого металла потенциал нулевого заряда свой.
Величина электродных потенциалов оказывает очень большое влияние на характер коррозионного процесса.
Скачок потенциала между двух фаз не может быть измерен, но при помощи компенсационного метода можно измерить электродвижущую силу элемента (ЭДС), который состоит из электрода сравнения (его потенциал условно принят за ноль) и исследуемого электрода. В качестве электрода сравнения берется стандартный водородный электрод. ЭДС гальванического элемента (стандартный водородный электрод и исследуемый элемент) называют электродным потенциалом. Электродами сравнения могут также выступать хлорсеребряный, каломельный, насыщенный медно-сульфатный.
Международной конвенцией в Стокгольме 1953г. решено при записях электрод сравнения всегда ставить слева. При этом ЭДС рассчитывать, как разность потенциалов правого и левого электродов.
Если положительный заряд внутри системы движется слева направо — ЭДС элемента считается положительной, при этом
где F — число Фарадея. Если положительные заряды будут двигаться в противоположном направлении, то уравнение будет иметь вид:
При коррозии в электролитах самыми распространенными и значимыми являются адсорбционные (адсорбция катионов или анионов на границе раздела фаз) и электродные потенциалы (переход катионов из металла в электролит или наоборот).
Электродный потенциал, при котором металл находится в состоянии равновесия с собственными ионами называется равновесный (обратимый). Он зависит от природы металлической фазы, растворителя, температуры электролита, активности ионов мет.
Равновесный потенциал подчиняется уравнению Нернста:
где, E ο — стандартный потенциал мет.; R — молярная газовая постоянная; n — степень окисления иона мет.; Т — температура; F — число Фарадея;αMe n+ — активность ионов мет.
При установленном равновесном потенциале электрохимическая коррозия не наблюдается.
Если по электроду проходит электрический ток — равновесное состояние его нарушается. Потенциал электрода изменяется в зависимости от направления и силы тока. Изменение разности потенц., приводящее к уменьшению силы тока, принято называть поляризацией. Уменьшение поляризуемости электродов называют деполяризацией.
Скорость электрохимической коррозии тем меньше, чем больше поляризация. Поляризация характеризуется величиной перенапряжения.
Поляризация бывает трех типов:
— электрохимическая (при замедлении анодного или катодного процессов);
— концентрационная (наблюдается, когда скорость подхода деполяризатора к поверхности и отвода продуктов коррозии мала);
— фазовая (связана с образованием на поверхности новой фазы).
Электрохимическая коррозия наблюдается также при контакте двух разнородных металлов. В электролите они образуют гальванопару. Более электроотрицательный из них будет анодом. Анод в процессе будет постепенно растворяться. При этом идет замедление или даже полное прекращение электрохимической коррозии на катоде (более электроположительном). Например, при контакте в морской воде дюралюминия с никелем интенсивно растворятся будет именно дюралюминий.
1. Положение металла в ряду активности металлов: чем дальше они расположены друг от друга тем быстрее происходит коррозия.
2. Чистота металла: примеси ускоряют коррозию.
3. Неровности поверхности металла , трещины
4. Грунтовые воды, морская вода, среда электролита.
5. Повышение температуры.
6. Действие микроорганизмов (грибы, бактерии и лишайники воздействуют на металл с высокой коррозионной стойкостью).
Термодинамика электрохимической коррозии
Стремлением металлов переходить из металлического состояния в ионное для различных металлов различно. Вероятность такого перехода зависит также от природы коррозионной среды. Такую вероятность можно выразить уменьшением свободной энергии при протекании реакции перехода в заданной среде при определенных условиях. Но прямой связи между термодинамическим рядом и коррозией металлов нет. Это объясняется тем, что термодинамические данные получены для идеально чистой поверхности металла, в то время как в реальных условиях корродирующий металл покрыт слоем (пленкой) продуктов взаимодействия металла со средой. Для расчетов изменения свободной энергии реакции при электрохимической коррозии металла используют величины электродных потенциалов. Следовательно, для электрохимического растворения металла необходимо присутствие в растворе окислителя (деполяризатора, который бы осуществлял катодную реакцию ассимиляции электронов), обратимый окислительно — восстановительный потенциал которого положительнее обратимого потенциала металла в данных условиях.
Катодные процессы при электрохимической коррозии могут осуществляться различными веществами.
3. оксидами и гидрооксидами (как правило малорастворимыми продуктами коррозии, образованными на поверхности металлов)
4. 4. органическими соединениями где R радикал или молекула
В коррозионной практике в качестве окислителей-деполяризаторов, осуществляющих коррозию, выступают ионы водорода и молекулы растворенного в электролите кислорода. При увеличении активности ионов металла (повышение концентрации ионов металла в растворе), потенциал анода возрастает, что приводит к торможению растворения металла. Понижение активности металла, напротив, способствует растворению металла.
Потенциал и ток коррозии. Поляризация в электрохимических процессах. Скорость процесса в соответствии с законом Фарадея. Экспериментальное определение скорости коррозии. Основные случаи возникновения коррозионных гальванических пар.
I — ток гальванического элемента
jок , jоа — электрохимические потенциалы соответственно катода и анода, определенные при условии холостого хода гальванического элемента (при I = 0 )
R — сопротивление цепи анод-среда-катод
h — смещение потенциала относительно своего равновесного состояния и обычно называемое перенапряжением процесса
A, B — некоторые константы, зависящие от параметров окружающей
среды и свойств металла
Rпол — сопротивление двойного электрического слоя металл-электролит
Э.Д.С. элемента тратится на преодоление омического сопротивления коррозионной среды в цепи между анодом и катодом и двух поляризационных сопротивлений
hк, hа — величина напряжения на поляризационном сопротивлении катода и анода соответственно
DUс — падение напряжения в коррозионной среде
Pк , Pа — удельные поляризационные сопротивления катода и анода, Ом . м 2
Rc — сопротивление среды между электродами, Ом

Е = jок — jоа — э.д.с. коррозионной гальванопары
hа, hк, DUc — напряжения участков цепи соответственно на поляризационном сопротивлении анода, катода и в среде между ними
Ø Чем больше ток поляризации ( I ), тем сильнее поляризуются — изменяют свой потенциал — электроды. При этом анод поляризуется положительно ( hа > 0 ), т.е. его потенциал становится более положительным, а катод — отрицательно, так как hк
Ø Ток коррозии Iкор зависит от разности электродных потенциалов (joa, jок ), которые, к сожалению, далеко не всегда известны, а не от потенциала коррозии jкор. Несмотря на свое имя, потенциал коррозии не определяет ток коррозии, а скорее наоборот: при токе коррозии Iкор устанавливается некий компромисный потенциал jкор.
Ø Ток коррозии тем выше, чем меньше поляризационное сопротивление. Очевидно, что ток коррозии тем выше, чем меньше сопротивление среды.
¨ ПОЛЯРИЗАЦИЯ В ЭЛЕКТРОХИМИЧЕСКИХ ПРОЦЕССАХ
Равновесные потенциалы электродов могут быть
определены в условиях отсутствия в цепи тока. При
прохождении электрического тока потенциалы
электродов меняются. Это явление называют
φi — потенциал электрода при прохождении тока
φр — равновесный потенциал (i = 0)
Любая электрохимическая реакция многостадийна.
1) подвод реагентов к электроду
2) собственно электрохимическая реакция
3) отвод продуктов реакции от электрода
возникновение поляризации обусловлено замедленностью отдельных стадий электрохимического процесса
Изменение потенциала электрода вследствие изменения концентрации реагентов в приэлектродном слое при прохождении тока называется концентрационной поляризацией.
Изменение потенциала, обусловленное замедленностью собственно электрохимических стадий реакций, называется электрохимической поляризацией (перенапряжением).
Закон Фарадея: количество электричества, стекающего с электрода, пропорционально потере массы этого электрода
G — масса растворившегося металла, г
q — электрохимический эквивалент металла, гA -1. ч -1
M — атомная масса, г/моль
F = 96500 — число Фарадея, Кл/г . Экв
n — валентность металла; I — величина электродного тока, А
плотность тока коррозии
j = I / S = G / (SqT)
практические формулы для расчета скорости коррозии
j – плотность анодного тока коррозии, А/м 2
v1 — скорость весовой коррозии, г/(м 2 ч)
v2 — скорость проникающей коррозии, мм/год
величина плотности анодного тока есть мера скорости коррозии
ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ СКОРОСТИ КОРРОЗИИ
По величине поляризационного сопротивления
Коррозиметры общего применения контролируют величину поляризационного сопротивления двух электродов датчика, погружаемых в коррозионную среду и подключаемых к внешнему источнику постоянного тока малого напряжения (U » 10 мВ). При этом измеряют наложенный ток пары ( I ), определяют поляризационное сопротивление
Rпол = U / I и, вводя некоторый поправочный коэффициент, находят скорость коррозии.
1. при измерениях фиксируют воздействие коррозионной среды на электроды датчика, но не на самое металлическое сооружение, ради которого проводятся измерения.
2. Метод не позволяет регистрировать какие-либо коррозионные гальванопары
Измеряют общую коррозию образца-свидетеля,
который помещают в коррозионную среду, по
возможности моделируя реальные условия
1. Метод широко применяется для лабораторных исследований, но мало пригоден для полевых.
Измерительными датчиками в данном случае являются
проволочные или иные элементы,сопротивление которых
увеличивается в процессе их коррозионного разрушения (за
счет уменьшения поперечного сечения). Коррозиметры,
построенные на этом принципе, — весьма точные электрические
измерительные приборы, позволяющие наблюдать коррозию
1. как и прочие методы измерения, регистрируют лишь коррозию датчиков, а не реального металлического сооружения.
Ультразвуковой контроль позволяет определять фактическую толщину стенки трубопровода или резервуара по изменению времени прохождения ультразвукового сигнала через стенку.
Радиографический контроль осуществляют с помощью рентгеновских лучей, “просвечивая” стенку резервуара или аппарата.
¨ ОСНОВНЫЕ СЛУЧАИ ВОЗНИКНОВЕНИЯ КОРРОЗИОННЫХ ГАЛЬВАНИЧЕСКИХ ПАР
Коррозия при контакте двух металлов
(-) Fe | водный раствор электролита | Cu (+)
(-) A (Fe) : Е°Fe/Fe2+ = -0,44 В
ЕH2/2H+(рН = 10) = -0,59 В
(+) K (Cu): ЕOH-/O2 (рН = 10) = +0,64 В
возможна коррозия железа только с кислородной деполяризацией, так как
Образующийся гидроксид железа (II) подвергается последующему окислению:
При этом образуется ржавчина (xFe2O3· yH2O).
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Как то на паре, один преподаватель сказал, когда лекция заканчивалась — это был конец пары: "Что-то тут концом пахнет". 8528 —  | 8115 —
| 8115 —  или читать все.
или читать все.
91.146.8.87 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно