- Содержание
- История [ править | править код ]
- Нахождение в природе [ править | править код ]
- Физические свойства [ править | править код ]
- Получение [ править | править код ]
- Химические свойства [ править | править код ]
- Применение [ править | править код ]
- Сведения о безопасности [ править | править код ]
- Нахождение в природе
- Физические свойства
- Получение
- Химические свойства
- Применение
- Сведения о безопасности
- Что это такое?
- Цены на сульфат калия
- Зачем нужен препарат?
- Признаки недостатка калия у растений
- Использование
- Для каких культур подходит?
- Калия сульфат и другие удобрения
- Цены на минеральные удобрения
- Хранение и меры предосторожности
- Видео — Калий и калийные удобрения
| Сульфат калия | |
|---|---|
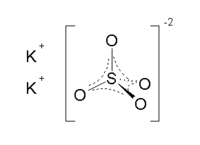 ( <<<картинка>>> ) |
|
 ( <<<изображение слева>>> ) ( <<<изображение слева>>> ) |
 ( <<<изображение справа>>> ) ( <<<изображение справа>>> ) |
наименование
(100 °C) 24 г/100 мл

Содержание
История [ править | править код ]
Сульфат калия был известен с начала 14-го века, изучен Глаубером, Бойлом и Тахеусом. В 17 веке он был назван arcanuni или sal duplicatum — эти названия были для кислот и щелочных солей.
Нахождение в природе [ править | править код ]
В природе находится на месторождениях калийных солей. Присутствует в водах солёных озёр.
Физические свойства [ править | править код ]
Бесцветные кристаллы, ромбическая сингония (a = 0,742 нм, b = 1,001 нм, c = 0,573 нм, Z = 4, пространственная группа Pnam). При температуре выше 584 °C переходит в гексагональную модификацию (a = 0,5947 нм, c = 0,8375 нм, Z = 2, пространственная группа P63/mmc).
Хорошо растворим в воде, не подвергается гидролизу. Нерастворим в концентрированных растворах щелочей или в чистом этаноле.
Получение [ править | править код ]
Минеральные формы чистого сульфата калия относительно редки. Минерал арканит (англ. Arcanite ) состоит из чистого K2SO4, представляет собой белые или прозрачные кристаллы, встречается в Калифорнии (США).
Есть много минералов, содержащих соли калия:
Промышленные методы получения основаны на обменных реакциях KCl с различными сульфатами и в результате сульфат калия, как правило, сильно загрязнён побочными продуктами:
2 K C l + 2 M g S O 4 ⇄ K 2 S O 4 ⋅ M g S O 4 + M g C l 2 <displaystyle <mathsf <2KCl+2MgSO_<4>
ightleftarrows K_<2>SO_<4>cdot MgSO_<4>+MgCl_<2>>>> 
ightleftarrows 2K_<2>SO_<4>+MgCl_<2>>>> 
ightleftarrows K_<2>SO_<4>+2NaCl>>> 
ightleftarrows K_<2>SO_<4>+CaCl_<2>+2H_<2>O>>> 
ightleftarrows K_<2>SO_<4>+FeCl_<2>>>>
Наиболее чистый продукт получают, обрабатывая твёрдый хлорид калия концентрированной серной кислотой:
100^
Прокаливанием с углём минерала лангбейнита:
T>>K_<2>SO_<4>+2Mgdownarrow +2CO_<2>uparrow +2SO_<2>uparrow >>>"> K 2 S O 4 ⋅ 2 M g S O 4 + 2 C → > T K 2 S O 4 + 2 M g ↓ + 2 C O 2 ↑ + 2 S O 2 ↑ <displaystyle <mathsf <2>SO_<4>cdot 2MgSO_<4>+2C<xrightarrow <>T>>K_<2>SO_<4>+2Mgdownarrow +2CO_<2>uparrow +2SO_<2>uparrow >>> 
В лабораторной практике применяют следующие методы:
- из оксида калия:
K 2 O + H 2 S O 4 → K 2 S O 4 + H 2 O <displaystyle <mathsf <2>O+H_<2>SO_<4><xrightarrow <>>K_<2>SO_<4>+H_<2>O>>>
- вытеснением из слабых или неустойчивых кислот:
K 2 C O 3 + H 2 S O 4 → K 2 S O 4 + C O 2 ↑ + H 2 O <displaystyle <mathsf <2>CO_<3>+H_<2>SO_<4><xrightarrow <>>K_<2>SO_<4>+CO_<2>uparrow +H_<2>O>>>
- из щёлочи и разбавленной кислоты:
2 K O H + H 2 S O 4 → K 2 S O 4 + 2 H 2 O <displaystyle <mathsf <2KOH+H_<2>SO_<4><xrightarrow <>>K_<2>SO_<4>+2H_<2>O>>>
- из гидросульфата калия:
2 K H S O 4 → 240 o C K 2 S O 4 + H 2 S O 4 <displaystyle <mathsf <2KHSO_<4><xrightarrow <240^

- окислением сульфида калия:
500^
- из надперекиси калия:
2 K O 2 + S → 140 o C K 2 S O 4 <displaystyle <mathsf <2KO_<2>+S<xrightarrow <140^
Сульфат калия получается при нагреве сульфита калия до температуры в 600 °C:
4 K 2 S O 3 → 600 o C K 2 S + 3 K 2 S O 4 <displaystyle <mathsf <4K_<2>SO_<3><xrightarrow <600^
K 2 C r 2 O 7 + S → 800 − 1000 o C C r 2 O 3 + K 2 S O 4 <displaystyle <mathsf <2>Cr_<2>O_<7>+S<xrightarrow <800-1000^
Взаимодействием сульфата аммония и гидроксид калия:
( N H 4 ) 2 S O 4 + 2 K O H → K 2 S O 4 + 2 N H 3 ↑ + 2 H 2 O <displaystyle <mathsf <(NH_<4>)_<2>SO_<4>+2KOH
ightarrow K_<2>SO_<4>+2NH_<3>uparrow +2H_<2>O>>>
Химические свойства [ править | править код ]
Как соль двухосновной кислоты образует кислые соли:
K 2 S O 4 + H 2 S O 4 ⇄ 2 K H S O 4 <displaystyle <mathsf <2>SO_<4>+H_<2>SO_<4>
ightleftarrows 2KHSO_<4>>>>
Как все сульфаты взаимодействует с растворимыми соединениями бария:
K 2 S O 4 + B a C l 2 → 2 K C l + B a S O 4 ↓ <displaystyle <mathsf <2>SO_<4>+BaCl_<2><xrightarrow <>>2KCl+BaSO_<4>downarrow >>>
Восстанавливается до сульфида:
K 2 S O 4 + 4 H 2 → 600 o C , F e 2 O 3 K 2 S + 4 H 2 O <displaystyle <mathsf <2>SO_<4>+4H_<2><xrightarrow <600^
С оксидом серы образует пиросульфат:
K 2 S O 4 + S O 3 → K 2 S 2 O 7 <displaystyle <mathsf <2>SO_<4>+SO_<3><xrightarrow <>>K_<2>S_<2>O_<7>>>>
Применение [ править | править код ]
Основной потребитель сульфата калия — сельское хозяйство. Сульфат калия является ценным бесхлорным удобрением. Эффективность сульфата калия лучше проявляется на бедных калием дерново-подзолистых почвах гранулометрического состава и торфяных почвах. На черноземных почвах он применяется обычно под культуры, которые усваивают много калия и натрия (сахарная свёкла, подсолнечники, плодовые, для корнеплодов, овощей). На каштановых и серозёмных почвах используют в зависимости от вида культуры, технологии выращивания и содержания калия в почве. Сульфат калия намного эффективнее влияет на величину урожая и его качество, если его применять в комплексе с азотными и фосфорными удобрениями. На кислых почвах действие сульфата калия повышается на фоне использования извести.
Калий повышает содержание сахаров и витаминов в выращиваемой продукции, а подкормки в конце августа-сентября способствуют лучшему зимованию плодово-ягодным и декоративным деревьям и кустарникам. Используется на различных почвах, под все культуры, а также для комнатного и балконного цветоводства. Сульфат калия пригоден для всех способов внесения: основного (при перекопке почвы весной или осенью) и для подкормки в течение вегетационного периода. [2]
Применяется в первую очередь под культуры, чувствительные к хлору (картофель, табак, лён, виноград, цитрусовые и др.). Наличие в удобрении сульфат-иона положительно влияет на урожай растений семейства крестоцветных (капуста, брюква, турнепс и др.) и бобовых, потребляющих много серы.
Также сульфат калия используется в производстве стекла, различных квасцов и других соединений калия, как флюс в металлургии. [3] В Европейском союзе допущен в качестве использования как пищевая добавка E515.
Сведения о безопасности [ править | править код ]
Следующие действия сульфатом калия на части тела могут вызвать:
- Глаза: попадание пыли может вызвать механическое раздражение,
- Кожа: попадание на кожу может вызвать раздражение,
- Проглатывание: употребление в пищу больших количеств может вызвать раздражениежелудочно-кишечного тракта,
- Вдыхание: при вдыхании может вызвать раздражение дыхательных путей,
- При хроническом употреблении сульфата калия: отравления могут возникать в редких случаях длительного воздействия.
Сульфат калия был известен с начала 14-го века, изучен Глаубером, Бойлом и Тахеусом. В 17 веке он был назван arcanuni или sal duplicatum — эти названия были для кислот и щелочных солей.
Нахождение в природе
В природе находится на месторождениях калийных солей. Присутствует в водах солёных озёр.
Физические свойства
Бесцветные кристаллы, ромбическая сингония (a = 0,742 нм, b = 1,001 нм, c = 0,573 нм, Z = 4, пространственная группа Pnam). При температуре выше 584 °C переходит в гексагональную модификацию (a = 0,5947 нм, c = 0,8375 нм, Z = 2, пространственная группа P63/mmc).
Хорошо растворим в воде, не подвергается гидролизу. Нерастворим в концентрированных растворах щелочей или в чистом этаноле.
Получение
Минеральные формы чистого сульфата калия относительно редки. Минерал арканит (англ. Arcanite ) состоит из чистого K2SO4, представляет собой белые или прозрачные кристаллы, встречается в Калифорнии (США).
Есть много минералов, содержащих соли калия:
Промышленные методы получения основаны на обменных реакциях KCl с различными сульфатами и в результате сульфат калия, как правило, сильно загрязнён побочными продуктами:





Наиболее чистый продукт получают, обрабатывая твёрдый хлорид калия концентрированной серной кислотой:
 100^oC> K_2SO_4+2HCluparrow>" border="0" />
100^oC> K_2SO_4+2HCluparrow>" border="0" />
Прокаливанием с углём минерала лангбейнита:
 T> K_2SO_4+2Mguparrow+CO_2+SO_2>" border="0" />
T> K_2SO_4+2Mguparrow+CO_2+SO_2>" border="0" />
В лабораторной практике применяют следующие методы:
- из оксида калия:

- вытеснением из слабых или неустойчивых кислот:

- из щёлочи и разбавленной кислоты:

- из гидросульфата калия:



- окислением сульфида калия:
 500^oC> K_2SO_4>" border="0" />
500^oC> K_2SO_4>" border="0" />
- из надперекиси калия:


Сульфат калия получается при нагреве сульфита калия до температуры в 600 °C:


Химические свойства
Как соль двухосновной кислоты образует кислые соли:

Как все сульфаты взаимодействует с растворимыми соединениями бария:

Восстанавливается до сульфида:


С оксидом серы образует пиросульфат:

Применение
Основной потребитель сульфата калия — сельское хозяйство. Сульфат калия является ценным бесхлорным удобрением. Эффективность сульфата калия лучше проявляется на бедных калием дерново-подзолистых почвах гранулометрического состава и торфяных почвах. На черноземных почвах он применяется обычно под культуры, которые усваивают много калия и натрия (сахарная свёкла, подсолнечники, плодовые, для корнеплодов, овощей). На каштановых и серозёмных почвах используют в зависимости от вида культуры, технологии выращивания и содержания калия в почве. Сульфат калия намного эффективнее влияет на величину урожая и его качество, если его применять в комплексе с азотными и фосфорными удобрениями. На кислых почвах действие сульфата калия повышается на фоне использования извести.
Калий повышает содержание сахаров и витаминов в выращиваемой продукции, а подкормки в конце августа-сентября способствуют лучшему зимованию плодово-ягодным и декоративным деревьям и кустарникам. Используется на различных почвах, под все культуры, а также для комнатного и балконного цветоводства. Сульфат калия пригоден для всех способов внесения: основного (при перекопке почвы весной или осенью) и для подкормки в течение вегетационного периода. [1]
Применяется в первую очередь под культуры, чувствительные к хлору (картофель, табак, лён, виноград, цитрусовые и др.). Наличие в удобрении сульфат-иона положительно влияет на урожай растений семейства крестоцветных (капуста, брюква, турнепс и др.) и бобовых, потребляющих много серы.
Также сульфат калия используется в производстве стекла, различных квасцов и других соединений калия, как флюс в металлургии. [2] В Европейском союзе допущен в качестве использования как пищевая добавка E515.
Сведения о безопасности
Следующие действия сульфатом калия на части тела могут вызвать:
- Глаза: попадание пыли может вызвать механическое раздражение,
- Кожа: попадание на кожу может вызвать раздражение,
- Проглатывание: употребление в пищу больших количеств может вызвать раздражение желудочно-кишечного тракта,
- Вдыхание: при вдыхании может вызвать раздражение дыхательных путей,
- При хроническом употреблении сульфата калия: отравления могут возникать в редких случаях длительного воздействия.
Даже хорошая плодородная земля на дачном участке с годами использования становится все беднее. Что уж говорить о скудных супесях и суглинках, в которых очень мало полезных и питательных веществ для растений. И выращиваемые вами культуры рано или поздно начинают испытывать недостаток того или иного элемента. Сульфат калия – удобрение, применение которого необходимо, чтобы восполнить в почве недостаток одного из главных элементов, нужных растению для роста и развития.
Что это такое?
Калия сульфат, также именуемый калием сернокислым – концентрированная подкормка для культурных растений, которая содержит элемент калий, необходимый для правильного и активного плодоношения и роста культур, выращиваемых как в открытом, так и в закрытом грунте. По внешнему виду это вещество выглядит как порошок белого цвета (с легким сероватым оттенком), состоящий из огромного числа крошечных кристаллов. Эти структуры горьковато-кислые на вкус и легко растворяются в воде.
В состав сульфата калия входят около 50% непосредственно самого калия, кислород, около 18% серы, немного магния – 3 %, кальция – 0,4%.
На заметку! Вредного и опасного хлора этот вид удобрений не содержит. Именно поэтому идеально подходит для тех растений, которые слишком чувствительны к хлору – например, бобовые и картофель.
Продается сульфат калия расфасованным в полиэтиленовые пакеты весом от 500 г до 5 кг. А приобрести его можно в любом садоводческом магазине, причем по доступной цене, что актуально для экономных и рачительных дачников, желающих создать своим зеленым насаждениям благоприятную среду обитания.
Цены на сульфат калия
Зачем нужен препарат?
Наличие калия как микроэлемента в почве очень важно для растений. Он регулирует их рост и развитие, важен для хорошего плодоношения. Именно благодаря ему в тканях растительных организмов на клеточном уровне проходят некоторые обменные процессы. Также калий повышает иммунитет культур, помогает им лучше переживать зимний период и положительно воздействует на циркуляцию воды в них, за счет чего питательные вещества, поступающие в корни, лучше и быстрее достигают листьев растений.
Калий – элемент плодородия, он не только улучшает плодоношение любого растения, но и повышает содержание витаминов и полезных для человеческого организма веществ.
На заметку! Раньше источником калия на садовом участке была древесная зола. Но, так как дровяные печи все больше уходят в прошлое, золу теперь мало кто хранит и делает специально. Намного проще купить удобрение с калием, например, сульфат калия. К тому же оно лучше, чем зола, растворяется в воде и проще применяется.
Калия сульфат как подкормка богат калием и является отличным источником этого элемента. Может применяться для выращивания растений как в закрытом, так и в открытом грунте, отлично подходит в качестве подкормки и комнатным цветам. Рекомендовано вносить его в почву, где растут культуры семейства Крестоцветные. Предпочитают сульфат калия баклажаны, перцы, огурцы. Будут благодарны за такое угощение и плодовые деревья и кусты – смородина, клубника, малина и другие. Удобрение подходит для любых типов почв, в том числе торфяных, песчаных, сероземных, подзолистых.
На заметку! Попадая в песчаный грунт, вещество легко курсирует в нем, но в суглинки для достижения наилучшего эффекта его рекомендуют вносить непосредственно туда, где располагаются корни растений.
Признаки недостатка калия у растений
Дефицит калия у растений выявить непросто, но на их состоянии это сказывается значительно. В зеленой части любого растительного организма в случае нехватки этого элемента наблюдается нарушение углеводного обмена, вследствие чего отмечается нарушение процесса образования крахмала и сахаров. Соответственно, некоторые культуры, такие как гречиха, картофель, кукуруза, становятся менее урожайными. У растений также снижается эффективность фотосинтеза и прочность зеленых частей.
Признаки того, что растения испытывают недостаток калия:
- медленный рост зеленой части;
- расстояние между междоузлиями у побегов уменьшается;
- листва желтеет, меняет форму, не может полностью развиться;
- быстро наступают некрозы листовых пластин;
- наличие точек, пятен белого/коричневого цвета на листьях;
- неактивное плодоношение;
- урожай плохо хранится;
- бутоны успевают засохнуть, даже не раскрывшись;
- повышается чувствительность к холодам.
Также у плодов растений, испытывающих нехватку калия, ухудшается вкус. Если вы заметили эти признаки на культурах, растущих на вашем огороде, и не хотите сгубить свои насаждения, то нужно принимать срочные меры – вносить удобрение сульфат калия.
Использование
Сульфат калия в качестве удобрения вносится в грунт различными способами – как в сухом виде, так и в виде водного раствора при поливе. Также он может применяться в качестве подкормки во время роста и развития растений на протяжении всего жизненного цикла. Раствором сульфата калия можно просто опрыскивать листья и стебли культур.
Большой эффективностью обладают все три вышеперечисленных способа внесения сульфата калия – полезные элементы, содержащиеся в удобрении, отлично усваиваются всеми частями растения. Хорошо применять подкормку в комплексе, но наибольший эффект обеспечивает, конечно же, внесение вещества непосредственно в грунт. Такой способ дает возможность не только подкормить растения, но и нормализовать химический состав земли на участке. Да и через корневую систему насаждения усваивают полезные элементы лучше.
Использовать сульфат калия очень просто – для этого не нужно обладать особыми знаниями и умениями.
Шаг 1. Весной или осенью перед перекапыванием земли на участке необходимо руками в перчатках разбросать удобрение в необходимом количестве, стараясь это делать равномерно.
Шаг 2. Во время перекопки грунта кристаллы сульфата калия нужно заделывать в почву, где происходит их растворение и превращение в другие химические вещества. Происходит нормализация кислотно-щелочного баланса грунта. При этом заделывать удобрение стоит примерно на ту глубину, на которой и залегает основная масса корневых систем.
На заметку! Осенью, при внесении удобрения в тяжелые грунты, старайтесь делать это на глубину побольше, а вот в песчаную почву сульфат калия заделывайте весной поближе к поверхности.
Шаг 3. Во время высадки в саду плодовых деревьев в ямы для корней стоит поместить сульфат калия вместе с фосфорным препаратом-подкормкой. Это обеспечит приток полезного элемента к корням растения, улучшит рост и развитие.
Шаг 4. Ежегодно процедуру внесения сульфата калия в грунт на огороде повторяют, чтобы постоянно восполнять количество калия. Это – залог хорошего урожая.
Шаг 5. Летом, во время второго внесения удобрений, растения подкармливают сульфатом калия, но уже в жидком варианте. Раствор, полученный в соответствии с инструкцией, вносят прямо под корень.
На заметку! Взрослое растение в саду можно подкормить через шурфы – отверстия в грунте, направленные под углом 45 градусов к корням. Прямо в эти отверстия и следует заливать разведенное удобрение в нужном количестве.
Таблица. Расход удобрения в зависимости от культуры при перекопке.
| Культура | Расход, г/м кв. |
|---|---|
| Томаты, огурцы, комнатные растения, цветы на участке | 15-20 |
| Клубника | 15-20 |
| Культуры, растущие в открытом грунте | 30-40 |
| Капуста, картофель, морковь, свекла | 25-30 |
| Плодовые деревья | 150-200 г на одну посадочную яму |
Таблица. Расход удобрения в зависимости от культуры во время роста.
| Культура | Расход, г/м кв. |
|---|---|
| Огурцы и томаты | 15-20 |
| Ягодные растения (лучше всего до начала цветения) | 15-20 |
| Корнеплоды | 30 |
| Клубника (период цветения) | 15-20 г |
| Капуста | 25-30 |
На грядках сульфат калия оптимально вносить на глубину около 8 см в междурядья. Если удобрение вносится в жидком виде, то обычно оно разводится в количестве 30-40 г на 10 л воды. Этого хватает примерно на 10-20 растений. Последний раз сульфат калия вносится примерно за две недели до сбора урожая.
На заметку! Помните, что при переизбытке калия особого вреда растениям нанесено не будет, но все же он (калий) будет препятствовать поглощению таких элементов как магний, кальций, марганец.
Для каких культур подходит?
Сульфат калия активно применяется при выращивания различных культур, его использование актуально для:
- бобовых, которым необходимо большое количество серы;
- крестоцветных (капусты, редиски, репы);
- растений, остро реагирующих на наличие хлора (картофель, цитрусы, табак);
- большинства корнеплодов;
- плодовых деревьев, а также кустарников;
- клубники;
- огурцов, томатов, перцев, баклажанов.
Стоит помнить, что количество удобрений и необходимость их внесения часто зависят от химического состава грунта. Знание того, какими элементами богата почва, может уберечь вас от ненужных трат.
Калия сульфат и другие удобрения
Данный препарат можно применять в комплексе с другими удобрениями. Например, калия сульфат можно использовать вместе с фосфатными или азотными подкормками. Такие тандемы не только питают почву и дают растениям необходимые полезные вещества, повышая их урожайность, но и отпугивают всевозможных вредителей. А для человека удобрения в дозах, не превышающих указанные в инструкциях по применению, неопасны. На кислых грунтах сернокислый калий можно вносить вместе с известью – так он будет работать эффективнее.
А вот соседство с мелом, мочевиной сульфат калия не приветствует, поэтому лучше использовать эти вещества по отдельности. Также сернокислый калий не используют, если применяют навоз, компост. Эти органические удобрения сами по себе обогащают почву калием, потому дополнительно его можно не вносить.
На заметку! Сульфат калия смешивают с азотными подкормками непосредственно перед внесением в грунт.
В магазинах часто можно найти комплексные удобрения, в которых сульфат калия соединен с фосфором, потому что именно вместе эти добавки работают отлично. Притом их воздействие на любое растение будет не только плодотворным, но и длительным.
Цены на минеральные удобрения
Хранение и меры предосторожности
Хранить сульфат калия следует в плотно закрытой таре в сухом помещении. Кстати, он со временем не слеживается, поэтому перед использованием мучиться с ним не придется – просто достается тара, далее по инструкции применяется вещество. Да и хранится удобрение в течение нескольких сезонов, не теряя своих свойств.
Так как сернокислый калий не относится к горючим веществам, его можно перевозить, не опасаясь, что он вспыхнет в любой момент.
На заметку! Помните, что при работе с сульфатом калия нужно соблюдать осторожность. Все же это — химическое вещество.
При попадании на слизистую оболочку носа, рта, глаз сульфат калия способен вызвать раздражение. Случаев отравления удобрением зафиксировано не было. Но все же во время работы с препаратом не трогайте глаза, не вдыхайте его, работайте в средствах индивидуальной защиты – респираторе, перчатках.
Следите, чтобы с удобрением не играли дети, чтобы до него не добрались домашние животные. Эксперименты с химией могут легко привести к беде.
Интересно, что сульфат калия бывает разных сортов. В одном из видов вещество содержит темные примеси, а непосредственно основного элемента в нем содержится несколько меньше. При этом подкормка не становится опасной при использовании в соответствии с той же инструкцией.
Почему трескаются помидоры в теплице
Поскольку растрескивание томатов не считается грибковым или инфекционным заболеванием овощей, то и обеззараживание не является панацеей от появления трещин на плодах. Однако проведение предпосевной обработки существенно повысит шанс получить здоровый урожай помидоров. Детальнее — в этой статье.
Сернокислый калий – одно из лучших и универсальных удобрений. Его можно применять не только на огороде, но и в домашнем цветнике. Комнатные растения начинают лучше расти и быстрее зацветают, так что остатки вещества, привезенные с дачи после окончания сезона, вполне можно использовать и дома. Также не стоит забывать регулярно применять сульфат калия на даче – пусть это будет неписанным правилом. Растения, получающие такую подкормку регулярно, отблагодарят вас прекрасным урожаем ягод, овощей и фруктов. Не зря препарат используют даже на сельскохозяйственных угодьях – фермеры, чей доход напрямую зависит от урожайности их плантаций, уже десятилетиями не изменяют сульфату калия, применяя его для своих насаждений.
